 |
Новости |  |
 |
Библиотека |  |
 |
Новые книги |  |
 |
Ссылки |  |
 |
Карта сайта |  |
 |
О нас |  |
 |

ХИМИЧЕСКИЙ ПАСПОРТ МОЛЕКУЛ(«Упрямый» прополис. — Отчего апельсин горький? — Грозные антибиотики и «увертливые» микробы.) Испытав в полной мере все взлеты и падения на тернистом пути исследователя, мы идентифицировали в конечном счете все девять компонентов самого распространенного в нашей стране типа прополиса. Формулы этих веществ приведены ниже (схема 6), они помогут нам разобраться в дальнейшем повествовании. Трудно переоценить информацию, содержащуюся в формуле каждого вещества. Любое природное соединение — это сама спрессованная эволюция, великий знак Природы. У вещества есть настоящее — его функция, прошлое — его история, путь его биосинтеза, «хозяева» — организм-продуцент и его ферментные системы, с «поточных линий» которых сошли молекулы. 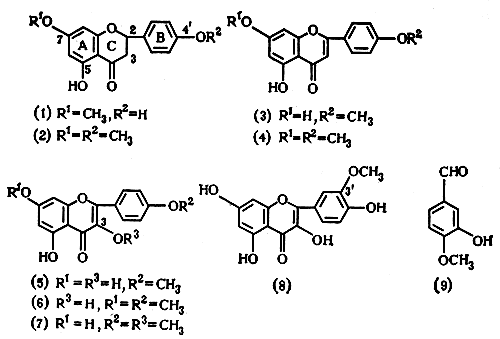 Схема 6. Структурные формулы соединений, идентифицированных в наиболее распространенном в СССР типе прополиса (1968): 1—2 — флаваноны; 3—4 — флавоны; 5—6 — флавонолы Проследим за тем, что скажут о прополисе формулы наших девяти соединений. Уже при первом взгляде на них даже не знакомому с химией человеку видно, что большинство веществ имеет явно родственную природу. При более внимательном рассмотрении обнаружатся и различия: неодинаковое число и характер функциональных групп (—ОСН3 и —ОН), наличие или отсутствие двойной связи в среднем кольце молекулы. Эти небольшие, казалось бы, изменения сильно влияют на многие характеристики вещества, в частности на хроматографическую подвижность и цвет пятен. Так, флаваноны (соединения 1—2) дают после опрыскивания пластинок концентрированной серной кислотой очень красивый ярко-оранжевый цвет; флавоны (3—4) и флавонолы (5—8) — желтый, переходящий со временем в коричневатый; особую окраску дает и девятое соединение — ароматический альдегид изованилин. Выделенные соединения хорошо кристаллизовались и имели довольно высокие температуры плавления. Это было удобно для очистки веществ и их идентификации. Однако и настораживало, потому что нас очень интересовало и «настоящее» выделенных соединений — их функции. Высокая же температура плавления могла свидетельствовать об их низкой растворимости в водных растворах, что серьезно осложнило бы оценку их биологической активности. К сожалению, наши опасения подтвердились: большинство соединений более или менее хорошо растворялось в органических растворителях (спирт, ацетон), но «не желало» переходить в водные растворы. Когда же мы их вынуждали к этому, добавляя к спиртовому раствору воду, они образовывали густые эмульсии. Работникам группы биологических испытаний, возглавляемой кандидатом биологических наук И. Д. Рябовой, пришлось немало потрудиться, чтобы получить воспроизводимые результаты. Они не вызвали энтузиазма: лишь некоторые вещества проявляли заметную антимикробную активность, например флавонол (7), против кислотоустойчивых бактерий и флавонон (1) — против патогенных грибов. Активность эта была в пределах 15—30 микрограммов на миллилитр. Ранее я занимался синтезом высокоактивных антибиотиков ряда тетрациклина и заинтересовался прополисом не только как интересным природным объектом, но и как продуктом, к которому не вырабатывается устойчивость (резистентность) микроорганизмов. Это очень важно, так как применение в медицине антибиотиков показало, что сила их резко идет на убыль. Причина этого очень тревожного факта заключалась именно в резистентности. Каким же механизмом или веществами владеют пчелы, что сумели избежать столь неприятного явления, сводящего на нет все усилия химиков и микробиологической промышленности? Каков принцип использования биологически активных антимикробных веществ в улье и есть ли они вообще в самом прополисе? На последний вопрос как будто бы уже ответили опыты Уайта, Лави, В. П. Кивалкиной и других исследователей, доказавших безусловную антимикробную активность экстрактов прополиса. Более того, идентификация некоторых биологически активных соединений показала, что активность прополиса можно связать и с конкретными соединениями, но она была по сравнению с антибиотиками невысокого уровня. И. Д. Рябова, также увлекшаяся идеей «рассекречивания» прополиса, была в явном замешательстве: исходный спиртовой экстракт прополиса заведомо активен, а выделить вещество активнее, чем сам экстракт, не удается. Прополис «не хотел» указать более активное вещество, чем он сам, хотя из большинства растений, например зверобоя, можно выделить активное начало, более эффективное, чем экстракт всего растения, где это начало разбавлено балластными для данной активности веществами. Та же ситуация характерна и для микроорганизмов: чтобы выделить тетрациклин, пенициллин, другой антибиотик, освобождаются от балластных веществ, образованных растущим мицелием. Ничего подобного с прополисом пока не происходило, хотя воображение рисовало очень заманчивую картину: найти соединения, прошедшие длительное «горнило» эволюционной проверки в весьма жестких условиях стесненного пчелиного пространства и заведомо безвредные для человека, поскольку он в течение тысячелетий систематически «вкушал» различные «изделия» пчел. Поэтому, когда на наших пластинках вспыхнул, наконец, всеми цветами радуги целый спектр соединений, было естественно надеяться найти среди них и эти «чудо-вещества». Это «чудо», однако, не состоялось. Тут мы стали догадываться, почему Мишель Барбье, прозанимавшийся прополисом 6—7 лет, явно охладел к нему: похоже, ученый тоже ожидал большей антимикробной активности. Капиталистические же фирмы, надо полагать, требовали реальных веществ. У нас, однако, никогда не угасала вера в «эволюционную мудрость» пчелы. «Улей-то — стерилен, в конце концов», — говорили мы себе, размышляя над выявленными фактами. Впрочем, ничего обескураживающего еще не было. Самые активные вещества могли прятаться среди тех, которые мы еще не выделили: девять компонентов далеко не исчерпывали химических ресурсов пчелиного клея. Судя по пятнам на пластинках, их было еще десятка два-три, если не больше. Однако при таком ходе рассуждений следовало признать, что эти главные по весовой доли вещества являются по сути бесполезными в защитной системе прополиса. Логика не допускала, что пчелы выбрали столь «разбавленный» по активности продукт. Пришлось вспомнить про синергизм. Так называется явление, когда отдельно взятое вещество само по себе малоактивно или неактивно вовсе, а в присутствии другого вдруг обнаруживает всплеск (резонанс) активности. Это предположение несколько утешало, но формулы веществ, которые мы к тому времени твердо установили, не давали особенно больших надежд и на явления синергизма. Дело в том, что флавоноиды, к которым относилось большинство идентифицированных в прополисе веществ, — очень распространенный класс природных соединений. Они встречаются почти во всех растениях, и уже одно это неопровержимо доказывает растительное происхождение основной части прополиса: ни животные, включая насекомых, ни микроорганизмы не способны синтезировать флавоноидный скелет молекулы. С другой стороны, флавоноиды — очень загадочные соединения. Несмотря на их многочисленность и распространенность, их функция в растениях до сих пор остается во многом неясной. Что же касается их действия на другие организмы, в частности антимикробной активности, то они, как правило, проявляют ее лишь в высоких концентрациях или не проявляют совсем. Идентификация большого числа флавоноидных соединений в прополисе вызвала и ряд других вопросов. Все вещества оказались в виде так называемых агликонов, то есть соединений, не содержащих сахарных остатков. В самих же растениях эти вещества, как правило, присутствуют именно в связанной форме или в форме гликозидов, когда к свободным гидроксильным группам молекулы присоединен один или больше остатков сахара, чаще всего глюкозы. Здесь можно вспомнить о горьком начале созревающих апельсинов — нарингине (схема 7). Он имеет при гидроксильной группе в положении 7 остаток глюкозы. От этой связи и зависит горький вкус плода, который исчезает при созревании (молекула разрушается, что приводит к освобождению агликона и глюкозы, а они уже не дают горького привкуса). Нарингин — пример обычной формы присутствия флавоноидов в растениях. 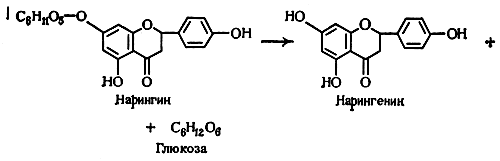 Схема 7. Гидролиз гликозида нарингина в тканях Почему же эти вещества в прополисе, если они попали в него из растений, утратили свои гликозидные «хвосты»? На все эти вопросы ответа пока не было. Тот факт, что флавоноиды оказались главными компонентами в наиболее распространенном в нашей стране типе прополиса, конечно, сильно поднимал их «авторитет» в наших глазах, но сравнение с антибиотиками было далеко не в пользу первых. Мы, однако, рассудили следующим образом: прополис, как уже стало очевидным, представляет собой очень сложную смесь соединений. Некоторые из них проявляют хотя и невысокую, но заведомую активность. При большой концентрации в прополисе этих соединений любой микроорганизм окажется в затруднительном положении. Почему? Представим сначала себе какой-либо антибиотик, например «исполин» типа тетрациклина или стрептомицина. Если мы подействуем этим сверхактивным веществом на колонию микроорганизмов, скажем, состоящую из 10 миллиардов отдельных клеток, то, как показывает практика, все они не погибают — всегда остается какая-то часть. Допустим, всего 10 клеток, но с них-то все и начинается! Эти микробы уже несут в себе тетрациклиноустойчивый участок в генетическом коде, и бесполезно на остаток колонии действовать новыми дозами антибиотика: они все равно не добьют оставшихся. Более того, последние могут еще более преобразоваться и даже начать употреблять антибиотик как пищу. Вот на что, оказывается, способны микроорганизмы!  Микробы способны на все Однако одолеть прополис микробам не удается: все попытки найти прополисоустойчивые штаммы, несмотря на многократные, тысячные пересевы любых типов микроорганизмов, оканчивались безрезультатно. Выходит, что тетрациклин, стрептомицин и подобные им «светила» антибиотического мира смертельно опасны для отдельных микроорганизмов, но сама популяция, если она достаточно велика, после первых «шоков» выживает, а впоследствии может даже и «не замечать» присутствия грозного врага. Как свидетельствует сохраняющаяся уже миллионы лет стерильность улья и безуспешность пересевов с целью получения устойчивых штаммов, прополис не дает невидимым вредителям таких шансов. Чем же берет микробов прополис? А вернее, что не позволяет им «взять» прополис? Испытанный нами уже на первых этапах работы флавонол (схема 6, 7) проявлял антимикробную активность против некоторых штаммов при концентрации 25—30 микрограммов в 1 миллилитре. Выделенный Барбье и Лави другой флавонол — галангин — имел подобный уровень активности. По сравнению с тетрациклином это в сотни раз меньше. Однако тетрациклин один, а соединений типа галантина в прополисе несколько. Это уже в 1964 году доказали опыты Барбье — Лави, которые, помимо галантна, выявили и еще одно антибактериальное вещество, впоследствии оказавшееся пиноцембрином. Эти вещества и многие другие, еще не идентифицированные, обладая различным химическим строением и, следовательно, неодинаковым механизмом антимикробного действия, совместно могли действовать намного успешнее «героя-одиночки» тетрациклина. Действительно, вероятность того, что колония микроорганизмов выработает механизм устойчивости одновременно к нескольким соединениям, намного ниже, чем к одному, даже самому активному соединению. Это, очевидно, и объясняет тайну устойчивости прополиса, словно бы «ощетинившегося» десятками различных соединений против любых типов микробов, посягающих на целостность провианта в улье и целебную чистоту его воздушной среды. Пчелам в конечном счете важнее надежность обороны, чем «личные» рекорды активности отдельных соединений. Такой вывод устроил нас на первых порах, и мы сосредоточили свое внимание на главном вопросе: откуда же в ульях берется этот загадочный чудо-продукт?.
|
 |
 |

ПОИСК:
|
 |
© PASEKA.SU, 2001–2019
Хаустова Наталья разработка оформления
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://paseka.su/ 'Paseka.su: Всё о пчеловодстве'
